Pesquisa publicada em 16 de abril na Frontiers in Microbiology analisou 493 animais silvestres entre 2020 e 2023. Dez deles traziam Klebsiella pneumoniae multirresistente. Uma raposa trazia também o gene blaNDM-5, que destrói carbapenêmicos.
Uma raposa encontrada morta na região da Emília-Romanha, no norte da Itália, carregava no intestino uma cepa de Klebsiella pneumoniae com o gene blaNDM-5. O gene produz uma enzima que neutraliza os antibióticos carbapenêmicos, classe que a Organização Mundial da Saúde considera criticamente importante e que costuma ser reservada para infecções hospitalares graves por bactérias já multirresistentes.
O que é blaNDM-5?
O blaNDM-5 codifica uma NDM-5, que é uma carbapenemase metalo-β-lactamase; na prática, isso significa que a bactéria pode inativar carbapenêmicos, antibióticos que costumam ser usados como recurso de última linha contra infecções graves por Gram-negativos. O texto de divulgação do estudo descreve essa enzima como uma variante que “can inactivate antibiotics”, e a literatura microbiológica já aponta o blaNDM-5 em isolados clínicos, animais e amostras ambientais, o que facilita sua disseminação entre bactérias.
O caso aparece em estudo publicado em 16 de abril na revista Frontiers in Microbiology. Os autores são pesquisadores do Instituto Zooprofilático Experimental da Lombardia e Emília-Romanha (IZSLER) e da Universidade de Parma, com primeira autoria de Maria Sampieri (IZSLER) e correspondência de Mauro Conter (Parma). O trabalho foi feito dentro do Plano Regional de Monitoramento da Fauna Silvestre da Emília-Romanha.
Entre agosto de 2020 e fevereiro de 2023, 493 animais silvestres encontrados mortos por trauma ou predação tiveram amostras fecais coletadas. O grupo incluiu 184 raposas-vermelhas (Vulpes vulpes), 123 pegas-rabudas (Pica pica), 86 gralhas-cinzentas (Corvus corone cornix) e 100 aves aquáticas de espécies como garças, cisnes, patos-reais, flamingos e pernilongos-de-costas-brancas.
Cinco espécies de Klebsiella nas amostras
Klebsiella spp. foi isolada em 32 amostras, o equivalente a 6,53% do total. Cinco espécies diferentes do gênero apareceram: 10 K. oxytoca, 10 K. pneumoniae, 6 K. variicola, 5 K. aerogenes e 1 K. quasipneumoniae.
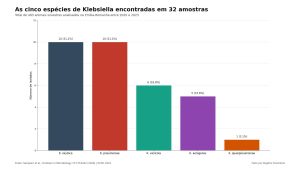
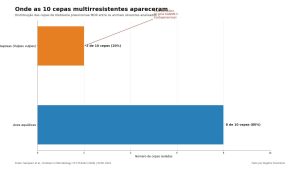
A prevalência de K. pneumoniae ficou em 2%, com intervalo de confiança de 95% entre 1% e 3,7%. Oito das dez cepas vieram de aves aquáticas e duas vieram de raposas. Das 32 Klebsiella isoladas, 14 (43,8%) se enquadraram na definição de multirresistência, ou seja, resistência a antibióticos de pelo menos três classes diferentes.
Perfil de resistência
As dez cepas de K. pneumoniae foram testadas contra 15 antibióticos. Todas apresentaram resistência a cefotaxima e ceftazidima, cefalosporinas de terceira geração usadas em meningites, endocardites e pneumonias bacterianas. Todas foram resistentes à ciprofloxacina, fluoroquinolona muito usada em infecções urinárias. Todas foram resistentes ao sulfametoxazol. Nove em dez foram resistentes à gentamicina.
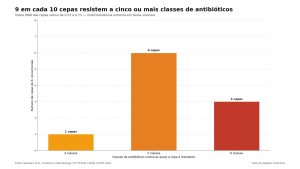
Os autores identificaram seis padrões distintos de resistência nas dez cepas. Uma delas resistiu a antibióticos de quatro classes; seis, a cinco classes; e três cepas, a seis classes diferentes. O índice MAR (Multiple Antibiotic Resistance), que mede a proporção de antibióticos aos quais o isolado é resistente dentro do painel testado, variou de 0,53 a 0,73 nas dez cepas de K. pneumoniae.
O relatório anual do Centro Europeu de Prevenção e Controle de Doenças (ECDC) publicado em 2024, referente a dados de 2023 sobre K. pneumoniae de pacientes humanos na Europa, mostra o contraste. Cefalosporinas de terceira geração: 100% nas cepas silvestres contra 19,6% dos isolados humanos na Itália e 9,3% na União Europeia. Fluoroquinolonas: 100% contra 17,4% na Itália e 8,8% na UE. Gentamicina: 90% contra 11,6% na Itália e 6% na UE.
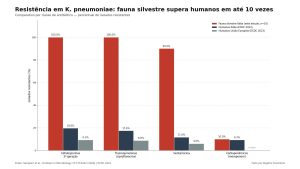
Os próprios autores ponderam que o dado não é diretamente comparável. O estudo usou meios de cultura seletivos para cefotaxima e carbapenêmicos, o que favorece o crescimento de cepas já resistentes e infla o percentual em relação a uma amostragem aleatória. Eles tratam o número como piso, não como média populacional.
A cepa da raposa e o gene blaNDM-5
Entre as dez cepas de K. pneumoniae, só uma também apresentou resistência fenotípica ao meropenem: a cepa 93, isolada de uma raposa. O sequenciamento completo do genoma mostrou que essa cepa carrega o gene blaNDM-5, responsável por uma metalobetalactamase do tipo New Delhi. A enzima é capaz de hidrolisar quase todos os betalactâmicos, inclusive carbapenêmicos como imipenem e meropenem.
O gene estava em um plasmídeo do tipo IncX3. Plasmídeos são moléculas circulares de DNA que podem passar entre bactérias diferentes, e o replicon IncX3 aparece com frequência na literatura internacional associado à família blaNDM em ambientes clínicos de Ásia, Europa e América Latina.
A linhagem ST307
Todas as dez cepas de K. pneumoniae pertencem ao sequence type ST307, clone que aparece em surtos hospitalares em pelo menos três continentes. González-Espinosa e colaboradores (2024) descreveram múltiplas introduções do ST307 em hospitais de Buenos Aires, na Argentina. Heiden et al. (2020) documentaram surto da mesma linhagem em hospitais alemães. Zhu et al. (2024) associaram o ST307 a surto por blaNDM-5 em Shanghai, na China. Os autores italianos citam essas publicações para contextualizar o achado na fauna silvestre.
Junto com o ST307 vieram os genes blaCTX-M-15, blaTEM-1D e blaSHV-28, todos ESBLs comuns em infecções humanas por enterobactérias em todo o mundo. As cepas também acumularam mutações nos genes cromossômicos gyrA e parC, que explicam a resistência a fluoroquinolonas mesmo sem a presença de genes plasmidiais.
Aves migratórias e raposas urbanas
Aves aquáticas migratórias cobrem grandes distâncias. Flamingos e cisnes, por exemplo, percorrem rotas internacionais que podem conectar zonas úmidas de países diferentes. Raposas-vermelhas circulam em raio curto. Frequentam áreas periurbanas, se alimentam de resíduos humanos e caçam pequenos mamíferos, o que as expõe a bactérias resistentes presentes em esgoto e cursos d’água contaminados, segundo os autores.
No artigo, os autores destacam que os dois grupos, por nunca receberem antibiótico diretamente, funcionam como amplificadores involuntários de cepas resistentes coletadas de fontes como estações de tratamento de esgoto e rios.
Limitações
Os pesquisadores apontam quatro limitações relevantes. As amostras vieram de animais encontrados mortos, o que introduz viés de sobrevivência. Os meios de cultura foram seletivos para resistência, o que infla o percentual de resistentes dentro do conjunto isolado. O desenho do estudo não permite estabelecer transmissão direta entre fauna silvestre e seres humanos. E o universo de dez cepas de K. pneumoniae, embora suficiente para análise genômica comparativa, é pequeno para inferência epidemiológica ampla.
O que isso significa para o Brasil?
Em 2019, Um trabalho brasileiro em Arq. Bras. Med. Vet. Zootec. já havia documentado Klebsiella pneumoniae multirresistente em animais domésticos e silvestres, incluindo isolados de origem animal processados em Cuiabá, mostrando que o país já tinha circulação desse problema em fauna.
Em 2013, a ANVISA emitiu alerta sobre NDM no país, indicando que microrganismos com esse mecanismo de resistência já exigiam atenção sanitária no Brasil.
O ponto de contato entre o estudo internacional e a realidade brasileira é a presença de reservatórios animais para bactérias resistentes. Se a fauna silvestre pode carregar clones de alto risco e genes como blaNDM-5 em outros países, o Brasil precisa considerar seriamente que esse tipo de resistência também pode circular em seus ecossistemas, sobretudo em zonas de interface entre cidades, rios, resíduos e áreas naturais.
Isso significa que a resposta sanitária não deve ficar restrita à microbiologia hospitalar. O problema passa a exigir monitoramento de fauna silvestre, água, esgoto, animais domésticos e cadeias de contato humano, porque a resistência aos carbapenêmicos reduz opções terapêuticas para infecções graves e aumenta o risco de disseminação regional.
A evidência mais forte aqui não é apenas a presença de uma bactéria resistente, mas a combinação entre espécie bacteriana, clone de risco e gene de carbapenemase. Quando esses três elementos aparecem juntos em fauna silvestre, o sinal é de circulação ecológica de resistência, o que amplia o problema para além dos limites dos serviços de saúde.
No caso brasileiro, o cenário pede cautela e vigilância contínua. O que o estudo sugere é que a fronteira entre ambiente e assistência está cada vez mais porosa, e isso torna a resistência antimicrobiana um tema de saúde pública e de gestão ambiental ao mesmo tempo.
Fonte: Wildlife as sentinel of antimicrobial resistance in Klebsiella spp. with genomic insights into Klebsiella pneumoniae in Northern Italy. Autores: Maria Sampieri, Lia Bardasi, Silvia Bonardi, Ilaria Menozzi, Alessandra Dodi, Erika Scaltriti, Giorgio Galletti, Elisa Massella, Cristina Bacci, Martina Rega e Mauro Conter. Publicação: Frontiers in Microbiology, v. 17, artigo 1716432, 16 de abril de 2026.
Leia também:
Por fragilidade energética, Petrobras estuda recompra da Rlam
Mercosul-UE entra em vigor em 1º de maio e pressiona Mato Grosso sob a Lei 12.709


















